スケルトンへの旅 石田 根吉 02/04/03
旅の始まり
それは僕にはとんでもない衝撃でした。昨年7月、本HPのLaboratoryのコーナーで余吾さんが紹介なさったホシテンスの幼魚の骨格透明標本を見た時の事です。
「何だこれっ? き、きれいだなあ~。こんなのどうしたら作れるんだろう?」
別に何を勉強しようという訳ではないのです。ただ、どうしても実物を自分の手で作り、自分の目で見たくなったのでした。幸い、簡単な薬品で作成できると書かれてあります。早速、この標本の作製法を書いた文献の紹介を余吾さんにお願いしました。間もなく送られて来たコピーは何と英文でした。
「うへ~っ」
こうして辞書を引きながらの長い長いスケルトンの旅が始まりました。それが昨年の8月末の事です。それ以降何度も失敗を繰り返し、漸く完成に漕ぎ付けたのは5ヶ月を経過した今年1月の事です。知らぬ間に5ヶ月が過ぎていました。
文献: G.Dingerkus and L.D.Uhler. 1977. Enzyme clearing of alcian
blue stained whole small vertebrates for demonstration of cartilage. Stain
Technol., 52: 229-232
参考HP:国立科学博物館
愛媛大学理学部
旅支度
まず、今回準備すべき薬品は以下の通りです(参考までに和光純薬から購入する時の入れ目と価格を添えておきました)。ほとんどは非常に一般的なもので、入手も簡単です。ただ、これらを全て一からそろえるとなると結構な出費となるでしょう。実際にはごく僅かしか必要ないのに、まとまった量で購入せねばならぬ薬品類も多くあるからです。
| 薬品名 |
入れ目 |
円 |
毒劇物指定 |
化学特性 |
| ホルマリン |
500ml |
680 |
劇物III |
腐食性 |
| 蒸留水 |
500ml |
850 |
|
|
| エタノール |
500ml |
2000 |
引火性 |
|
| 酢酸 |
500ml |
1400 |
危-4-2-III |
引火性 |
| アルシャンブルー8GX |
5g |
3300 |
|
|
| ホウ酸ナトリウム |
500g |
940 |
|
|
| トリプシン |
25g |
2300 |
|
|
| アリザリンレッドS |
25g |
3900 |
|
|
| 水酸化カリウム |
500g |
920 |
劇物II |
腐食性 |
| グリセリン |
500ml |
1450 |
危-4-3-III |
|
| 過酸化水素水 |
500ml |
1600 |
劇物II |
酸化性 |
| チモール |
25g |
1050 |
有毒性 |
腐食性 |
幸い僕は化学系の職場に居る為にほとんどの薬品は手許にあり、よって、その・・・今回は・・・会社に協力願ったと言いますか・・。コホン。
また、法律上は毒劇物に指定されているものもあるので、扱いや保管、廃棄に注意が必要なのは言うまでもありません(実際はそれほど怖い薬品はありません)。
このほかに必要な器具として、魚を処理する容器が必要です。僕は、近所の100円ショップで800ml容量のタッパを5~6個買ってきました。その他に、薬剤を保管しておくガラス瓶や、容量を測るメスシリンダーの様なものもあった方がよいのですが、なければ適当な台所用品で済んでしまいます。
旅立ち
以下、上記文献の操作手順(1)~(10)に沿って作成法をご紹介します。各手順の訳の後に僕が感じた注意点を書き添えてあります。
まず、作業に入る前に、文献には書かれていない注意より。
透明標本にどんな大きさの魚を選ぶかはかなり重要な要素です。僕は初め15cm程度はあるムツで挑戦したのですが、かなりてこずった末に失敗してしまいました。まずは全長10cm程度の魚を選ぶのが適当でしょう。しかも、それを5~6匹揃えたほうが無難です。万一、1匹で失敗してもすぐに補充できますし、途中で処理条件を何通りかに振って進める場合にも余裕を持って臨めます。
では、今回は10cm程度のマアジを例に取ってお話を進めます。
(1) 新鮮なサンプルをホルマリンに2~3日以上漬けて固定する。
「ホルマリン固定」という言葉を聞いた事はあってもそんな処理を行うのは今回が初めてでした。「固定」と言うのは「腐敗の進行を停止させる」という意味かと思っていたのですが、本当にカチンコチンに固まってしまうのです。ホルマリン入ったビンに魚を無理矢理押し込んで、後ほど取り出して見たら体が弓なりになって固まっていたことがありました。ホルマリン固定には十分な大きさの容器を用意しましょう。
 図1. ホルマリン固定中のマアジ
図1. ホルマリン固定中のマアジ
また、文献ではこのホルマリン固定の後に魚の内臓を取り出す事になっていますが、その前に処置しておくほうがよいと思います。固定後は身が堅くなって非常に作業がし辛く、骨を傷つけてしまいそうでした。また、初めに体を開いておく事でホルマリンの浸透も効率的になるのではないでしょうか。
ハリセンボンの透明標本化を試みて、まずそのまま固定しようとした事がありました。が、体腔の空気が抜けきらなかったせいで十分に固定が進行せず、後になって怪しげな体液が滲み出してきた事がありました。初めから体を開いていればよかったのです。
尚、以後の操作ではすべて、6匹(合計100g)のマアジに対して500mlの薬液を用いて処理を進めています。
(2) 蒸留水を何度か交換しながら2~3日掛けて洗浄する。できるだけこの段階で皮を剥ぎ、内臓を取り出しておいたほうがよい。
皮を剥ぐのは、ホルマリン固定後の方が確かに綺麗に出来る様に感じました。また、少々小さな魚でも出来る限り皮は剥いでしまった方がよいと思います。全長7cm程度のクロホシイシモチの透明標本作製に挑んだ折、
「こんなに小さいんだから皮を剥いだら却って体を傷つけてしまう
だろう」
と考えてこの手順を飛ばしたために、透明化に大層時間を要した事がありました(その上、結局最終段階で失敗してしまいます。後述)。面倒くさがらずに丁寧に皮を除きましょう。但し、頭部は薄い頭骨と皮がかなり密接にくっ付いているので、皮がある程度残るのは仕方ないと思います。

図2. この程度まで皮を剥ぐ
(3) 10mgのアルシャンブルー8GN、80mlの95%エタノール、20mlの氷酢酸の混合溶液に標本を漬けて24~48時間放置する。硬骨魚類の骨は軟骨から硬骨になっていくものと、直接硬骨として形成されるものがあります。幼期には軟骨部が残っているので、それをアルシャンブルーで青く染めようとするのです。硬骨は、後から加えるアリザリンで赤紫に染めてやります。
上記の混合溶液は合計100mlの場合ですので、実際に使用する液の量に応じて同一の割合で調製します。

図3. アルシャンブルー粉末を加えたところ
(4) サンプルを95%エタノールに移し、2~3時間おきにそのエタノールを2度入れ替える。(5) 以後、75%エタノール、40%、15%へと2~3時間おきに順に移していく。
(6) 最後に蒸留水に移して2~3時間放置する。
以上の操作は面倒くさいのですが、辛抱強く一歩ずつ。また、文献には2~3時間おきと書いてありますが、仕事を持っている人間がマアジの傍で番をしている訳にも行きませんので、或る時は半日また或る時は1日ほったらかしという事もありました。
旅の難所
(7)30mlのホウ酸ナトリウム飽和溶液、70mlの蒸留水、1gのトリプシン混合溶液に標本を漬ける。液が青っぽくなったり、2~3日経過したら溶液を交換する。こうして、真骨や軟骨がはっきり見えるようになり、筋肉の青みがきえるまで処理を続ける。それには普通2~3週間を要する。
さあ、愈々透明化のプロセスに差し掛かりました。タンパク質の分解酵素であるトリプシンを作用させるという化学反応を行っているのですから、温度の影響をかなり強く受けます。真夏ならばよいのですが、今頃の冬の季節ですとこの透明化が室温ではなかなか進みません(我が家にはエアコンもストーブも無いものですから・・)。そこで、容器ごと電気コタツの中に入れる事にしました。なるほど、これだと快調に反応が進んでいるようです。
ただし、このコタツ処理には重要なポイントがあります。まず、コタツの設定は「弱」です。そして、容器はコタツの隅の方に置きましょう。つまり、余り温度を上げ過ぎてはいけないのです。
それを気付かずに加熱しすぎて、もう間もなく透明化が終了する標本の身がボロボロに剥がれ落ちて液が真っ黒に濁ってしまった事がありました。つまり、反応が暴走してしまったのです。折角のここまでの苦労も水の泡となってしまったのです。ですから、家族から不満が出ようと、子供が風邪をひこうと、コタツの設定は「弱」なのです。なんだったら接着剤で固定しましょう。
また、透明化が進むと共に、ホルマリン固定で固まっていた魚の体がドンドン柔らかくなっていきます。ですから、液を代えたり容器を移す時にはグローブをして自分の手で直接扱いましょう。それを知らずに、クロホシイシモチをピンセットで摘んで、尾鰭が千切れたことがありました。かなり時間の掛った標本だっただけに泣くに泣けませんでした。
更に、液をどういうタイミングで交換していったらよいのかが文献からはよく分かりません。

図4. トリプシン溶液交換のタイミング
僕は上の写真の様に、液がやや黄褐色に色づいて来た段階を交換のタイミングと判断しました。コタツの中でおよそ2日位です。
また、上の写真では、皮を剥いでから処理したものと皮を残したままのものを比較用に並べてあります(トリプシン処理4日後)。皮を剥いだ物は早くも透明化の兆しがあるのに対し、皮を残した物はまだ全然変化が無いのがお分かりいただけると思います。
更に難しいのが、「透明化処理をいつ打ち切るか」という判断です。長々と引っ張っても身が軟らかくなっていくばかりですし、早過ぎると透明化という目的が達成できません。その為に、複数の標本を順番に引き上げて行くのがよいでしょう。
今回のばあいは、下に示した「透明化処理10日後」が最適でした。

図5. 透明化処理の打ち切りのタイミング
透過光で見て骨が見える程度で、「これで本当に大丈夫か」と不安だったのですが、この後のプロセスで透明化は更に進行するので、この段階ではこれで十分なようでした。
(8) 水酸化カリウムの0.5%溶液にアリザリンレッドSをくわえて濃紫色の溶液を作る。ここに標本を入れて24時間放置する。
アリザリンを一体どれ位加えればよいのか分からないので困りました。染色剤は少量でも十分に効力を発揮するので、500mlの液に耳掻き一杯でも多い位でしょう。
(9) サンプルを 0.5%KOH溶液:グリセリン=3:1 + 3%過酸化水素水3~4滴の液に漬ける。続いて、0.5%KOH溶液:グリセリン=1:1
+ 3%過酸化水素水3~4滴、更に0.5%KOH溶液:グリセリン=1:3へと移していく。
この段階での水酸化カリウムの作用で透明化が更にゆっくり進みます。ですから、この処理の時間を自在に前後させて透明化の進行をコントロールする事ができます。
(10) 標本を純粋グリセリンに移す。更に防黴用にチモールの結晶を加えておく。
旅の終わり
こうして、透明骨格標本の長い長い旅が終わりました。最後に僕の手許に残ったのが下の写真の様な小さなマアジでした。

図6. マアジの透明骨格標本
前から後ろから上から横から飽かず眺めてはため息がでます。
「綺麗だなあ」
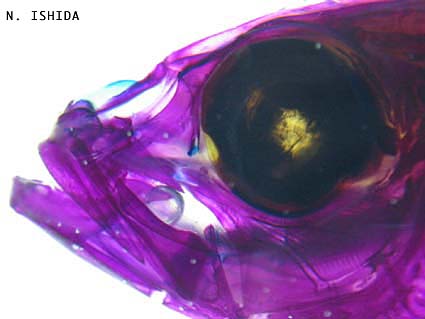
図7. マアジの頭部
これが頭部の拡大写真です。アリザリンにより赤紫に染まっているのが硬骨で、アルシャンブルーで青く染色される軟骨は殆どありません。魚の頭が如何に複雑な骨の組み合わせで出来ているのかがよく分かります。精緻なガラス細工を見るようですね。

図8 マアジの肩帯と腰帯
胸鰭部分には、所謂「鯛のタイ」と呼ばれる肩甲骨と烏口骨のつながりが見えます(この場合は「鯵のアジ」でしょうか)。普通は焼き魚か煮魚をさばかなければ取り出せないのにさすが透明標本です。

図9 マアジの尾部
そして、僕が最も気に入ったのがこの写真です。以前、BBSでも話題になりましたが、尾鰭を支える尾骨です。棘の一本一本がその尾骨に繋がっている様子までもよく分かりますね。
「それにしても綺麗だ」
ここに至るまでの手間と時間を思うと一層いとおしさが募ります。この日、穏やかな心持ちで、久々に深い眠りに就けた僕でした。何度も挫けそうになる度に的確なアドバイスを頂いた余吾さん、どうもありがとうございました。
事務局より:僕は恐竜発掘のテレビ番組や本が好きです。化石の骨に肉付けをしてはるか昔に生きていた恐竜たちを再現していく作業を楽しみながら、良く復元できるものだと関心します。
魚類の骨格標本作りは、この逆の作業をして行くわけですが、専門家になると、骨と筋肉や内臓との関係を見ながら、ばらしていくのですね。この骨や筋肉を動かして、喰ったり、ケンカしたり、子を作ったりしているのですね。まあ、当たり前と言えば、当たり前ですが。
こうして骨を眺めていくと、今まで図鑑などで抵抗を感じた骨の名称もなんとなく身近に感じられるようになるのではないかなと思います。
スケルトンへの旅ー番外編
透明標本は壊れやすく、グリセリンの中に保存するので、写真を撮るにも苦心するはずと思い、質問しました。以下のご返事でした。紹介します。これがまた、面白い。
実は、この部分にはさほどの工夫はありません。
今回、撮影はすべてデジカメで行いました。(実売3万円程度の普及版です)
ポリプロピレン製のタッパウェアにグリセリンと標本を入れ、それをスライド写真用のビューワーの上に置いて透過光を主な光源として撮影しました。但し、それだけだと影が少し強すぎるので、上から電気スタンドの光を反射光用に当てました。透過光:反射光=3:1程度の割合がよかったようです。
上述のように今回の光源はすべて蛍光灯です。従来のリバーサル・フィルムなんかですと蛍光灯光源で撮影すると仕上がりが青っぽくなってしまいます。ところが、最近のデジカメは大抵、光源による色温度の補正がカメラ側でセット出来るようになっていますので便利です。
また、拡大撮影の場合。通常のデジカメですとあそこまで倍率を上げることはできません。そこで、今回は、これまた100円ショップで買ってきた虫眼鏡をレンズの前に手持ちでセットしました。
撮影には三脚は用いず、すべて手持ちで行いました。但し、手ぶれを防ぐために、カメラ側のISO感度を200~400相当に設定しました。こうして7~8枚撮れば、1枚位は満足いくカットが取れます。残りは消去すればよいのですから、デジカメならではの利点と言えますね。
更に、カメラ側の自動露出ですと、透過の白色光を強く感じて絞りすぎてしまいます。そこで、露出を1段~2段開けてやるように補正すると骨の色が綺麗に見えました。
僕は今も銀塩フィルムが好きで、これを捨てるつもりは全くないのですが、今回のような場合はデジカメの有り難みを改めて感じました。